Introducción
La osteoporosis es una enfermedad sistémica ósea que se caracteriza por una disminución de la cantidad y/o calidad del hueso1. Su principal consecuencia son las fracturas por fragilidad, debidas a traumatismos de baja energía2, 3. Estas fracturas suponen una carga para la sociedad y para el individuo: aumentan el gasto económico de los sistemas sanitarios, generan dolor crónico, incapacitación, e incluso la muerte1, 3, 4.
El progresivo envejecimiento de la población acentúa este problema, situándolo como una prioridad sanitaria3, 4. Las discrepancias en las recomendaciones disponibles dificultan el manejo de esta enfermedad3, provocando un infratratamiento en la prevención secundaria de la fractura osteoporótica donde la terapia es más costo-efectiva.
El objetivo de esta revisión es analizar la evidencia disponible con respecto al tratamiento de la osteoporosis en el adulto para determinar a quién tratar, con qué, y durante cuánto tiempo.
Identificación de la población de riesgo: factores de riesgo de fractura
Los principales factores de riesgo de fractura por fragilidad están expuestos en la Tabla 1. Entre los factores de riesgo comunes, en las diferentes guías están: la edad, los antecedentes (familiares y personales) de fractura, el tabaquismo, el bajo índice de masa corporal, las caídas, y algunas enfermedades y fármacos. En los hombres existe menos información, pero se han identificado muchos de estos mismos factores de riesgo5. En general, la existencia de alguno de estos factores de riesgo debe poner en alerta sobre un peligro de fractura, y la presencia de varios correspondería con un aumento aditivo de dicho riesgo.
Tabla 1. Factores de riesgo de osteoporosis y fractura por fragilidad reflejados en las guías clínicas y en la escala de riesgo FRAX
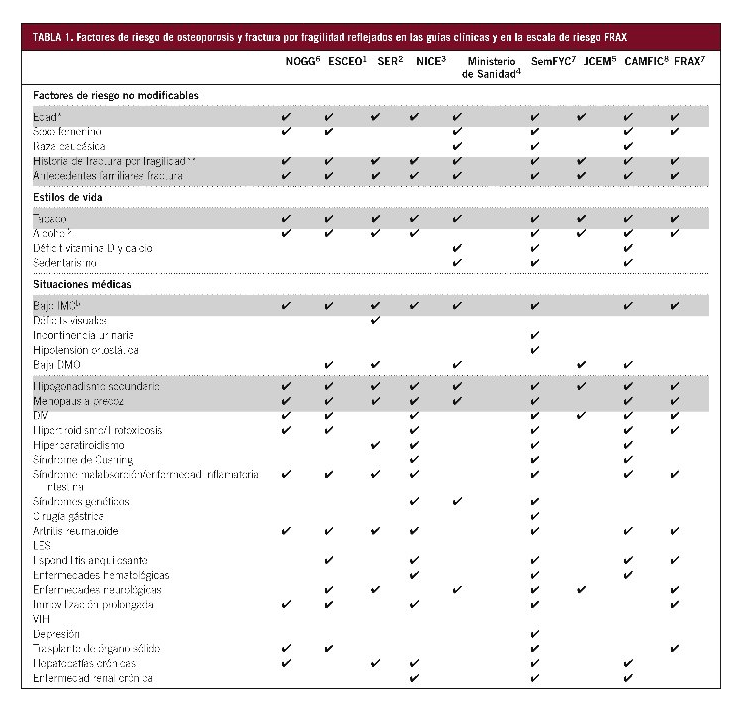

*Edad: > 65 años mujer, > 75 años hombre.
**Fracturas a partir de los 40-45 años4.
§Alcohol: > 3 UI/día (FRAX), > 14 UI/semana en mujeres o > 21 UI/semana en hombres3.
bIMC: < 18,5 kg/m2 (NICE), < 19 kg/m2 4,6, < 20 kg/m2 (SER).
aConsumo de corticoides: > 5 mg prednisona o equivalente más de 3 meses2,7, cualquier dosis vía oral durante más de 3 meses6.
En sombreado están los factores de riesgo comunes a todas las guías y al FRAX.
CAMFIC: Societat Catalana de Medicina Familiar i Comunitària; DM: diabetes mellitus; DMO: densidad mineral ósea; EPOC: enfermedad pulmonar obstructiva crónica; ESCEO: European Society for Clinical and Economic Aspects of Osteoporosis and Osteoarthritis; JCEM: Endocrine Society Journals and Publications; IBP: inhibidores de la bomba de protones; IMC: índice de masa corporal; ISRS: inhibidores selectivos de la recaptación de serotonina; LES: lupus eritematoso sistémico;
NICE: National Institute for Health and Care Excellence; NOGG: National Osteoporosis Guideline Group; SemFYC: Sociedad Española de Medicina de Familia y Comunitaria; SER: Sociedad Española de Reumatología; VIH: virus de la inmunodeficiencia humana.
A quién tratar:
Valoración del riesgo de fractura. Selección de la población que se ha de tratar según los factores de riesgo

Prevención secundaria
Existe consenso a la hora de determinar que los individuos con antecedentes personales de fractura por fragilidad tienen un mayor riesgo de refractura, por lo que muchas guías consideran que la población con antecedente previo de fractura osteoporótica o “por fragilidad” (producida tras una caída desde la propia altura o menor) debería ser tratada directamente sin necesidad de realizar otras evaluaciones1, 2, 5, 6, 7, 8.
Prevención primaria
La mayor parte de guías contemplan que los individuos con factores de riesgo considerados de alto riesgo deberían recibir tratamiento; sin embargo, identificar cuáles o cuántos de estos factores de riesgo marcan el umbral de tratamiento es más complicado, y arbitrario. La nueva guía de osteoporosis publicada en 2014 por la Societat Catalana de Medicina Familiar i Comunitària8 recomienda tratar en prevención primaria a pacientes con 2 o más factores de riesgo y un T-score < –3 (en pacientes menores de 65 años) o < –2,5 (en casos de 65 años o más).
Selección de la población que se ha de tratar según el FRAX
La Organización Mundial de la Salud desarrolló en 2008 la herramienta FRAX (http://www.shef.ac.uk) para el cálculo del riesgo de fractura total y de cadera en los próximos 10 años.
Actualmente no existe una recomendación común para el cribado de la osteoporosis en la población general, sin embargo se aconseja utilizar el FRAX en todos los pacientes mayores (mujeres ≥ 506 o ≥ 65 años3 y en hombres mayores ≥ 70-75 años3, 5) y en aquellos con algún factor de riesgo de fractura1, 2, 5, 6, 7. Entre las limitaciones del FRAX destacan que solo utilice los valores de la densitometría de fémur y la no contabilización del número de caídas, fracturas previas o dosis de corticoides, infravalorando el riesgo en estos pacientes1, 7. En la Tabla 2 están reflejados unos baremos de corrección que se publicaron a posteriori para subsanar algunas de estas limitaciones9.
![]()
Tabla 2. Ajuste del riesgo de fractura a 10 años del FRAX en función de la diferencia entre la densitometría ósea de columna y de fémur y en función de la dosis de corticoides vía oral.
| Ajuste de riesgo de fractura según diferencia entre DXA columna y DXA fémur | ||
| +/-10% por cada DE de diferencia entre las 2 localizaciones | ||
| Ajuste de riesgo de fractura según dosis de corticoides | ||
| Dosis de prednisona o equivalente (mg/día) | Ajuste medio sobre todas las edades | |
| Riesgo de fractura de cadera | < 2,5 | 0,65 |
| 2,5-7,5 | No ajustar | |
| ≥ 7,5 | 1,20 | |
| Riesgo de fractura total | < 2,5 | 0,8 |
| 2,5-7,5 | No ajustar | |
| ≥ 7,5 | 1,15 | |
DXA: densitometría ósea.
Tabla adaptada5 con el permiso de Springer Science + Business Media B.V.
![]()
El FRAX divide a los individuos en 3 grupos de riesgo (alto, moderado o bajo). Los puntos de corte que separan cada grupo dependen de factores tanto epidemiológicos como económicos, por lo que deben ser adecuados para cada país1. Actualmente no existen baremos adecuados a la población española, aunque algunas guías clínicas han utilizado unos puntos de corte aproximados2, 7. El estudio de cohortes en la población española FRIDEX objetivó una infraestimación del riesgo de fractura con estos puntos de corte, por lo que propuso unos más adecuados para la población española (pendientes de validación en una cohorte independiente)4, 7. En la Figura 1 podemos ver los grupos de riesgo según el FRAX y el FRIDEX7.
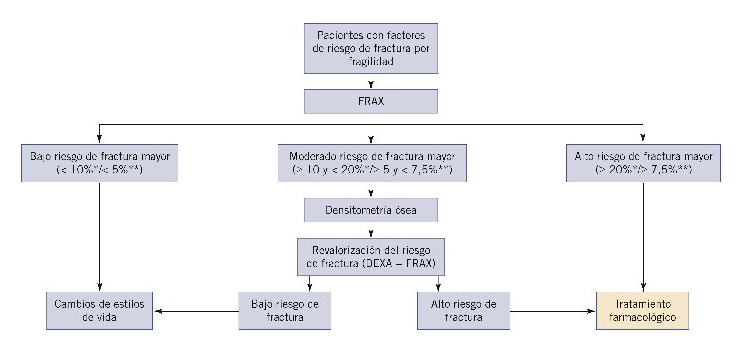
Figura 1. Algoritmo para la valoración del riesgo de fractura mayor según el FRAX.semFYC: Sociedad Española de Medicina de Familia y Comunitaria; Sociedad Española de Reumatología.*Puntos de corte aproximados reflejados en la SER y semFYC.**Puntos de corte del estudio FRIDEX.
Según la densitometría ósea
La densitometría ósea es considerada el Gold standard para el diagnóstico de la osteoporosis por su alta especificidad, sin embargo su baja sensibilidad hace que la recomendación de tratamiento únicamente basada en la densitometría sea cada vez menos recomendada en las guías clínicas1, 6, 7, 8. Además, esta herramienta no está universalmente disponible en todos los países, su interpretación depende de la edad, de los factores de riesgo2, y los puntos de corte de tratamiento dependen del sistema sanitario de cada país1.
Tratamiento (no farmacológico y farmacológico) para reducir el riesgo de fractura
Medidas no farmacológicas
Las medidas no farmacológicas deberían ser recomendadas a todos los pacientes que presenten factores de riesgo y especialmente a todos los que estén en tratamiento para la osteoporosis. Entre estas se encuentran la práctica de ejercicio físico1, 2, 5, 7, 8, la eliminación de hábitos tóxicos5, 7, 8, la prevención de caídas1, 2, 6, 7, 8, la corrección de los defectos visuales y un aporte adecuado de calcio y vitamina D1, 6, 7, 8.
El calcio y la vitamina D han sido fármacos ampliamente prescritos en población general como tratamiento preventivo, sin embargo, esta práctica ha sido cuestionada recientemente a raíz de la posible asociación entre el consumo de calcio y la cardiopatía isquémica4. Varias guías han modificado en consecuencia su sugerencia inicial, recomendando ahora aumentar el consumo de calcio en la dieta1, 5, 6, 7, 8y suplementando solo en casos de déficit1. Las dosis recomendadas oscilan entre 1.000-1.200 mg/día de calcio y entre 400-800 UI de vitamina D al día1, 7, 8. En los hombres con factores de riesgo u osteoporosis se recomiendan estas mismas dosis de calcio y suplementos de vitamina D suficientes para mantener unos niveles de 25(OH)D de al menos 30 ng/ml en sangre5, 8.
Medidas farmacológicas para reducir el riesgo de fractura
Nos centraremos únicamente en analizar las fracturas que previenen cada uno de los principales tratamientos y la evidencia disponible sobre la priorización entre ellos.
En la Tabla 3 están reflejados los principales tratamientos disponibles. La falta de estudios comparativos hace que la priorización entre fármacos no esté unánimemente reflejada en la literatura. La elección del fármaco que se ha de usar se debería realizar con base en su coste-efectividad y en el perfil del paciente, ya que existen indicaciones y contraindicaciones diferentes para los diversos medicamentos disponibles8.
![]()
Tabla 3. Tratamientos farmacológicos para la osteoporosis según la fractura que previenen, la duración máxima según los principales ensayos clínicos
| Fármacos | Fractura vertebral | Fractura no vertebral | Fractura de cadera | Duración máxima de tratamiento (años)δ |
| Alendronato | + | + | + | 10 |
| Risedronato | + | + | + | 7 |
| Ibandronato | + | +* | – | 3 |
| Ácido zoledrónico | + | + | + | 6 |
| Denosumab | + | + | + | 6 |
| Ranelato de estroncio | + | + | +** | 10 |
| Teriparatida | + | + | – | 2 |
| Raloxifeno | + | +b | – | 8 |
| Bazedoxifeno | + | +b | – | 5 |
δDuración máxima del seguimiento en ensayos clínicos 2,4,8 .
*Solo en subgrupo de riesgo alto.
**Solo en subgrupo de alto riesgo (> 70 años con DEXA femur < -3 DE).
βEn subgrupo de mujeres de alto riesgo (DEXA ≤ –3 DE o ≥ 1 fractura vertebral).
![]()
En todo caso, la mayoría de guías recomiendan los bifosfonatos orales como tratamientos de primera línea2, 4, 6, 7, especialmente el alendronato y el risedronato2, 6, debido a su alto coste-efectividad.
En la mayoría de casos, el zoledronato y el anticuerpo monoclonal denosumab compiten como fármaco de segunda línea, recomendados ambos en casos de intolerancia gastrointestinal o en caso de estar contraindicados los bifosfonatos orales. El primero se usa en infusiones endovenosas anuales (administración hospitalaria principalmente) y el segundo es de uso subcutáneo semestralmente (atención primaria/hospitalaria).
El ranelato de estroncio1, 4, 6, el raloxifeno y el bazedoxifeno son considerados tratamientos de tercera línea1, 2, 4, 6debido tanto por sus limitaciones sobre prevención de fractura de cadera como por sus efectos secundarios y contraindicaciones.
La teriparatida se reserva en la mayoría de guías para pacientes con muy alto riesgo de fractura, especialmente para aquellos con antecedentes de > 1 fractura vertebral2, 5.
En el hombre, los únicos tratamientos recomendados son el alendronato5, el risedronato, el ácido zoledrónico, la teriparatida2, 5 y el denosumab5.
Dado que la mayoría de ensayos clínicos de estos fármacos se llevaron a cabo junto con la administración de calcio y vitamina D, muchas guías recomiendan su suplementación en todos los pacientes que estén en tratamiento antirresortivo2, 4, 7.
Monitorización del tratamiento
El efecto de los antiresortivos sobre el hueso es modesto, por lo que los intervalos entre las densitometrías óseas deben ser suficientemente grandes para poder ver diferencias. Las recomendaciones a la hora de realizar los controles densitométricos en pacientes con tratamiento para la osteoporosis varían entre los 1,5-5 años1, 2, 8 con múltiples discrepancias a la hora de valorar la monitorización en las osteoporosis secundarias2, 4.
Duración del tratamiento y revaluación
En la Tabla 3 podemos ver la duración máxima aprobada para los tratamientos antiosteoporóticos. No obstante, la revaluación de dichos tratamientos debería llevarse a cabo antes; el alendronato2, 4, 6, el risedronato o el ibandronato a los 5 años4, 6 y el ácido zoledrónico a los 3 años, además de volver a revaluar al paciente siempre que haya cambios en los factores de riesgo6.
La aparición de efectos secundarios al tratamiento ha llevado al planteamiento de la supresión temporal de estas medicaciones aprovechando el efecto residual que tienen en el hueso; este concepto se denomina “vacaciones terapéuticas”. De esta manera, el alendronato podría ser suspendido durante 1-3 años, el risedronato o el ibandronato durante 1-2 años, y el ácido zoledrónico durante 2-3 años sin perjuicio esperado para el paciente. Transcurrido este plazo, se debería hacer una nueva evaluación del riesgo para valorar si se reintroduce la medicación o no6. Es necesario remarcar la falta de datos sobre la eficacia o seguridad de esta estrategia, así como la difusión de datos recientes (en congresos especializados) que apuntan a un incremento del riesgo durante este período de “vacaciones”. Es por tanto relevante utilizar esta estrategia (si se hace) con cautela y rigor, y solo en pacientes con un riesgo reducido después de tratamiento. A modo de ejemplo, el estudio FLEX (extensión del ensayo clínico FIT) demostró que tras 5 años de alendronato, las pacientes que tenían osteoporosis densitométrica, el tratamiento con 5 años más tenía efectos beneficiosos8.
Unidades especializadas en el manejo de las fracturas por fragilidad
El diagnóstico y seguimiento de la osteoporosis en nuestro país es coordinado por múltiples especialidades. A pesar de que es una enfermedad prevalente y que sus consecuencias generan una alta morbimortalidad, el manejo del paciente con una fractura por fragilidad sigue siendo subóptimo; solo un 20% de los que sufren una fractura de cadera inician tratamiento antiosteoporótico para prevenir nuevas fracturas, por lo que mejorar este porcentaje de tratamiento se ha convertido en una prioridad sanitaria10.
Para poder paliar este déficit, algunos países, como el Reino Unido, han creado unidades especializadas en la atención al paciente fracturado llamadas Fracture Liason Services. Estas unidades, formadas por medicina y/o enfermería, se encargan del seguimiento del paciente a partir del momento de la fractura. Analizan los factores de riesgo que han llevado a este paciente a fracturarse, aseguran el inicio del tratamiento e inciden en el cumplimiento terapéutico. Los buenos resultados obtenidos en pacientes fracturados (incremento del tratamiento hasta en un 90%10) nos indican que la idea de la priorización de la prevención secundaria del paciente fracturado, sea en el formato que sea, podría ser útil también en España.
Errores frecuentes
- Utilizar solo la densitometría como único método de valoración de riesgo de fractura.
- No tratar farmacológicamente las fracturas por fragilidad (prevención secundaria).
- No valorar el tratamiento en función con base en su coste-efectividad y el perfil del paciente.
- Dejar el tratamiento farmacológico indefinido sin revalorarlo.
Puntos clave
- La edad, los antecedentes familiares y personales de fractura, el índice de masa corporal bajo, el número de caídas, algunas enfermedades y fármacos son factores de riesgo clave de osteoporosis y de fractura/s por fragilidad.
- La evaluación del riesgo de fractura puede realizarse a través de la valoración de dichos factores de riesgo, mediante el cálculo del FRAX, o con una combinación de ambos.
- Los bifosfonatos orales son los tratamientos de primera línea, siempre y cuando no existan contraindicaciones.
- Las unidades de prevención secundaria de fracturas han mejorado la identificación y manejo de los pacientes con fractura por fragilidad en otros países, y podrían ser de utilidad en España.
Carlen Reyes Reyesa, Daniel Prieto Alhambraba
a Grupo de Investigación GREMPAL (Grup de Recerca en Malalties Prevalents de l’Aparell Locomotor). IDIAP Jordi Gol. Barcelona. España
b Investigador Sénior. Unidad de Epidemiología Músculo-Esquelética. Nuffield Department of Orthopaedics, Rheumatology, and Musculoskeletal Sciences. University of Oxford. Reino Unido
Formación Médica Continua Marzo 2015
1.Kanis JA, McCloskey EV, Johansson H, Cooper C, Rizzoli R, Reginster JY. Scientific Advisory Board of the European Society for Clinical and Economic Aspects of Osteoporosis and Osteoarthritis (ESCEO) and the Committee of Scientific Advisors of the International Osteoporosis Foundation (IOF). European guidance for the diagnosis and management of osteoporosis in postmenopausal women. Osteoporos Int. 2013; 24:23-57.
2.Pérez Edo L, Alonso Ruiz A, Roig Vilaseca D, García Vadillo A, Guañabens Gay N, Peris P, et al. Spanish Society of Rheumatology. Actualización 2011 del consenso Sociedad Española de Reumatología de osteoporosis. Reumatol Clin. 2011; 7:357-79.
3.National Institute for Health and Care Excellence. Osteoporosis: assessing the risk of fragility fracture. CG146. Londres: National Institute for Health and Care Excellence; 2012.
4.Batista Calvo JC, Carbonell Abella C, Valdés , Llorca C. Guía de la buena práctica clínica: osteoporosis postmenopaúsica prevención de fracturas por fragilidad. Ministerio de Sanidad, Política Social e Igualdad. IMC. Madrid. 2011.
5.Watts NB, Adler RA, Bilezikian JP, Drake MT, Eastell R, Orwoll ES, et al. Osteoporosis in men: an Endocrine Society clinical practice guideline. J Clin Endocrinol Metab. 2012; 97:1802-22.
6.Compston J, Bowring C, Cooper A, Cooper C, Davies C, Francis R, et al. National Osteoporosis Guideline Group. Diagnosis and management of osteoporosis in postmenopausal women and older men in the UK: National Osteoporosis Guideline Group (NOGG) update 2013. Maturitas. 2013; 75:392-6.
7.Gallo Vallejo F, Medina Abellán M, Giner Ruiz V, Nieto Pol E, León Vázquez F, Pérez Martín A, et al. Osteoporosis Manejo: prevención, diagnóstico y tratamiento. Barcelona: Semfyc Ediciones; 2014.
8.Azagra R, Carbonell C, Hoyo J, Iglesias M, Martínez-Laguna D, Montero JC, et al. Guia d’Osteoporosi. 2.a ed. Barcelona: EdiDE SL; 2014.
9.Kanis JA, Johansson H, Oden A, McCloskey EV. Guidance for the adjustment of FRAX according to the dose of glucocorticoids. Osteoporos Int. 2011; 22:809-16.
10.Eisman JA, Bogoch ER, Dell R, Harrington JT, McKinney RE, McLellan A, et al. ASBMR Task Force on Secondary Fracture Prevention. Making the first fracture the last fracture: ASBMR task force report on secondary fracture prevention. J Bone Miner Res. 2012; 27:2039-46.





Sin Comentario